



 首页
/ 新闻中心 / 不溶性微粒应用专题 | 如何检测微球中的不溶性微粒
首页
/ 新闻中心 / 不溶性微粒应用专题 | 如何检测微球中的不溶性微粒
新闻中心
不溶性微粒应用专题 | 如何检测微球中的不溶性微粒
 2026-04-28
2026-04-28

不溶性微粒应用专题 | ALP_AN_228_CN_如何检测微球中的不溶性微粒
奥法美嘉微纳米应用工程中心 - 陈祎园

本文隶属于不溶性微粒应用专题,全文共 5101字,阅读大约需要 16 分钟
摘要:随着生物医药技术的发展,以PLGA为代表的聚合物微球制剂作为长效缓释复杂注射剂,其临床应用日益广泛。不溶性微粒作为影响微球制剂临床安全的关键因素,是质量控制的核心环节。当前全球主流药典推荐光阻法(LO)作为不溶性微粒检测第一法,但微球本身的粒径与不溶性微粒检测范围重叠,易造成检测干扰。本文结合USP <1788> 法规建议,系统阐述微球中不溶性微粒的检测挑战,提出溶剂溶解前处理、MFI正交验证、模拟灌装验证三大核心检测策略。研究表明,溶剂溶解前处理结合高精度光阻法,辅以MFI正交验证,是解决微球检测干扰的最优路径,可为微球制剂质量控制及合规申报提供坚实的技术支撑。
关键词:微球;不溶性微粒;光阻法;流动成像显微镜;质量控制
近年来,随着生物医药技术的演进,以脂质体、微球为代表的复杂注射剂(Complex Injectables)应用日趋广泛[1]。其中,微球制剂通常由可生物降解的聚合物(如聚乳酸-羟基乙酸共聚物,PLGA)构成,能够将多肽、蛋白质等脆弱的活性分子包裹其中,实现数周至数月的长效缓释。
然而,无论剂型如何革新,不溶性微粒的检测与控制始终是保障临床安全的基石。各国药典规定,注射剂中的不溶性微粒是指非故意引入、不溶于药液且无法被机体代谢的微小颗粒。相关临床研究表明,一旦这些微粒随注射进入人体,极易引发静脉炎、局部肉芽肿;对于微球常用的肌肉或皮下注射途径,异常的亚可见微粒(Sub-visible particles)甚至可能诱发严重的免疫排异反应或局部组织坏死[2]。因此,如何准确表征和控制不溶性微粒,是确保微球制剂质量不可或缺的环节。

目前,全球主要药典(如 USP <788>、ChP <0903>等)均将光阻法(Light Obscuration, LO)作为检测不溶性微粒的第一法定方法。光阻法凭借卓越的定量准确性、极佳的重复性和法规符合性,是日常质控和合规申报的首选。
但复杂注射剂由于制剂配方的复杂性,会产生大量固有微粒(即微球本身)。通常,微球的粒径分布在1~500μm之间(常见为10~100μm),而药典规定的不溶性微粒常规检测指标针对≥10μm和≥25μm的微粒。显然,这些微球的粒径正好处于不溶性微粒的常规检测范围内。如果直接将混悬液进行检测,微球本身也会被传感器计入,导致严重的重合误差,呈现出完全失真的高数据量[3]。
要破解这一难题,常规的光阻法仪器往往力有不逮。成功的检测方案必须满足几个苛刻条件:
第一,需能处理经有机溶剂前处理后的特殊样品体系,对仪器的耐腐蚀性和进样精度要求极高;
第二,在微球溶解后可能存在的复杂本底中,仪器需具备极高的分辨率与灵敏度,以准确捕捉微量外来微粒;
第三,整个方法必须完全符合药典法规要求,确保数据合规有效。
如何在海量的微球本底中,精准识别出极少量的有害外来微粒(如环境纤维、包材脱落物、金属碎屑等),已成为了微球质控的行业痛点。
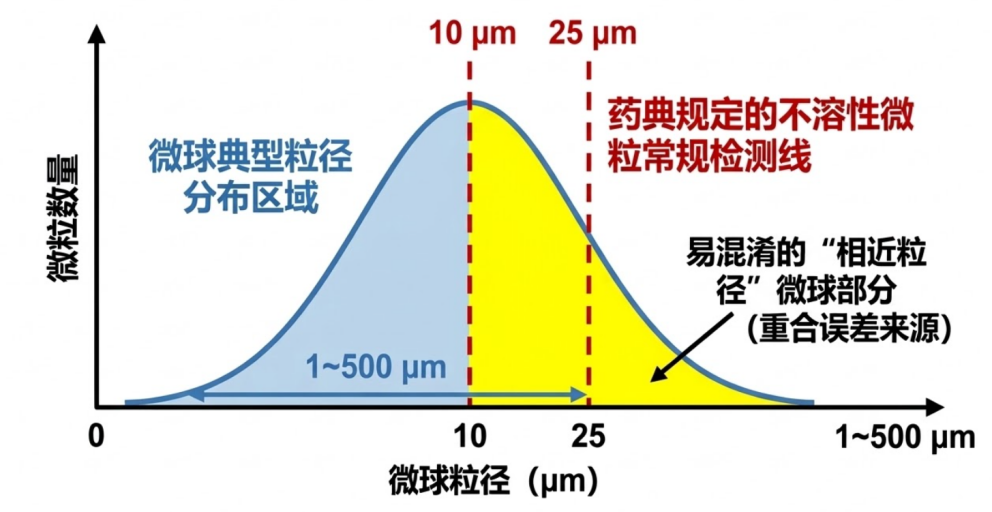
图1 微球粒径与不溶性微粒检测标准重叠示意图

针对由于本身特性与不溶性微粒检测范围重叠的挑战性样品,USP <1788> 给出了一些测试和前处理建议[4]:
使用溶剂溶解所有产品固体后,再进行微粒测定。
使用离心法将产品固体与载体分离。
使用特定筛网或筛子将产品固体与产品载体分离,以尽量减少干扰。
使用替代性澄清流体(如无菌培养基或盐水)评估产品灌装系统。

结合USP <1788> 的测试建议和微球制剂本身特性,在实际研发和质量控制中,通常采用以下三大检测策略:
1、基于溶剂溶解的前处理破坏法(主流推荐)
针对微球这类基质,既然微球本体会对检测造成干扰,那就通过前处理技术将其去除。可以寻找一种特定的有机溶剂,能够完全溶解聚合物微球骨架(如PLGA),同时保证不溶解外界引入的硅油、玻璃碎屑、不锈钢颗粒或纤维等不溶性杂质[5]。
在实际的文献与应用中,这种基质溶解策略已被广泛证实:
有机溶剂萃取与溶解: Park等在关于PLGA长效注射剂的研究中指出,溶剂的选择至关重要,诸如二氯甲烷(DCM)、乙酸乙酯或二甲基亚砜(DMSO)等有机溶剂能高效破坏PLGA的高分子酯键结构,使原本浑浊的微球悬液转变为澄清溶液,从而暴露内部或外部的不溶性杂质[5]。
绿色溶剂与衍生物溶解:除了传统毒性溶剂,近期 ACS Omega发表的研究证实,如乳酸乙酯(Ethyl lactate)等绿色溶剂同样具备优异的 PLGA 溶解能力[6]。
此外,也有专利与研究提出使用特定的水溶性聚乙二醇(PEG)衍生物溶液来温和地溶解聚合物微球载体[7]。
基质溶解后,外来不溶性微粒完好保留在澄清溶液中,此时再接入光阻法设备进行检测,即可获得真实合规的污染数据[8]。需要极其注意的是,采用此方法必须使用经过高精度(如0.22μm)过滤的洁净溶剂以避免引入新的微粒干扰,且必须进行充分的方法学回收率验证。
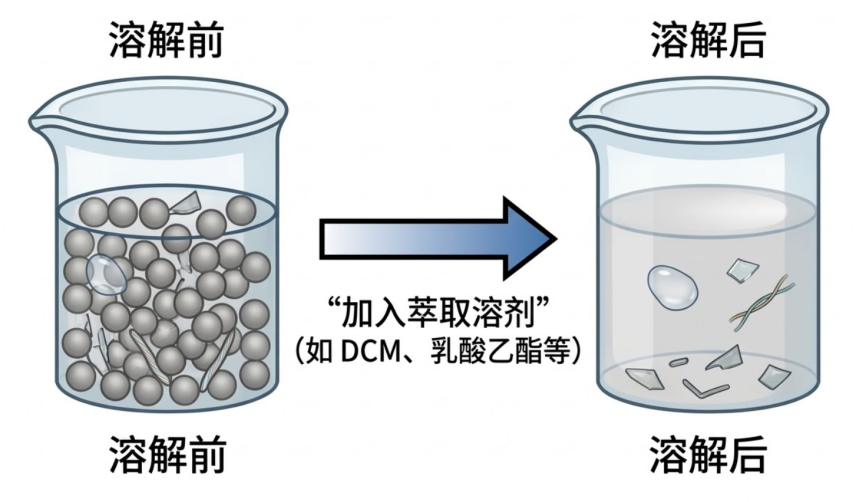
图2 应对微球高本底干扰的检测策略图
2、引入正交验证技术(MFI)
如果强行溶解会导致体系变化或缺乏合适的溶剂,可以引入流动成像显微镜(MFI)等新技术进行正交验证,能够更精准地表征不溶性微粒,USP 1788 中也将流式成像(FI)法列为了列为评估亚可见微粒的重要补充方法。
流式成像显微镜技术(MFI)不仅能统计粒子数量,还能获取流通池中每一个粒子的形态参数(如长径比、圆度)。PLGA微球通常呈规则的圆球状,而外界混入的玻璃碎屑或环境纤维形状极不规则,通过软件设定形态学筛除条件,可精准剥离出微球基质,实现对异常杂质的单独计数。
3、模拟灌装验证法(替代澄清流体法)
当直接测试成品存在困难时,可以采用过程控制的思路。使用不含聚合物微球的缓冲液或无菌生理盐水作为替代性澄清流体,完全模拟微球的配液、灌装、压塞等生产操作过程。收集完成模拟灌装的替代流体,对其进行标准的光阻法测试。只要证实整条生产线工艺设备、内包材(西林瓶、胶塞)在运行中不会引入超标的外来微粒,结合对原材料的微粒控制,就可以从某种程度上侧面论证最终微球药品的微粒安全性。
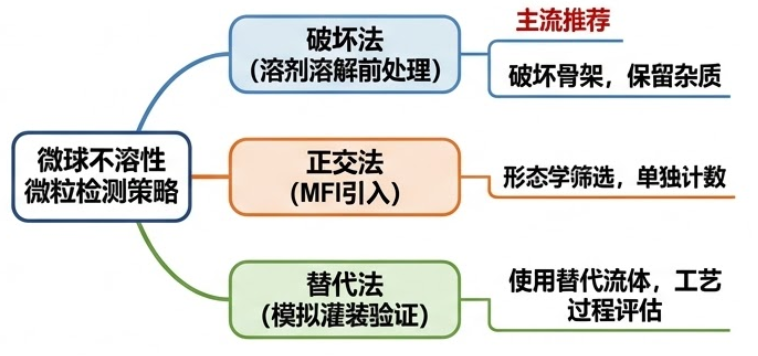
图3 应对微球高本底干扰的检测策略图

针对上述微球不溶性微粒检测的三大核心难点(基质干扰、样品珍贵、法规严苛),在微球不溶性微粒的检测和合规申报等场景中,选择一台能够应对复杂前处理样本的光阻法设备至关重要。AccuSizer A2000 USP不溶性微粒检测仪凭借其独特的设计,完美契合了复杂制剂的检测需求:
直击微量痛点:微球样品经特殊溶剂溶解后,体系往往较为昂贵,或存在挥发、腐蚀等风险。传统设备需要数毫升的进样量,而A2000USP不溶性微粒检测仪依靠先进的注射泵进样系统,最小进样量低至 50μL。
高分辨率与宽量程:设备采用单颗粒光学传感计数SPOS技术,融合光阻效应与光散理论。检测范围覆盖 0.5-400μm,拥有1024个高分辨率数据通道。
法规符合性:软件全面符合 FDA 21 CFR Part11 及 cGMP 规范,内置 ChP、USP、EP 等多国药典标准报告一键生成功能。



图4 AccusizerA2000USP不溶性微粒仪

总结
微球制剂作为新型复杂注射剂,其不溶性微粒的精准检测与控制是保障临床用药安全的关键,也是制剂质量控制和合规申报的核心要求。当前微球不溶性微粒检测的核心难题在于其自身的高本底干扰。
结合 USP <1788> 法规的前处理建议,采用溶剂溶解前处理法去除微球基质干扰,随后接入高精度光阻法进行检测,是目前最具科学依据与法规依从性的主流推荐方案。在研发异常排查时,辅以 MFI 正交验证技术进行形态学区分,可进一步提升检测的准确性。选用微量进样、高分辨率且合规的专用检测设备(如 AccuSizer A2000),将为微球制剂的不溶性微粒检测提供最强有力的技术保障,筑牢复杂制剂的质量防线。
参考文献
[1] Panchal, K., Katke, S., Dash, S. K., et al. (2023). An expanding horizon of complex injectable products: development and regulatory considerations. Drug Delivery and Translational Research, 13(2), 433-472.
[2] Sediq, A. S. (2024). Analysis of sub-visible particles in complex injectable formulations. Scholarly Publications, Leiden University.
[3] Zhu, Y., et al. (2024). Machine Learning-Enabled Image Comparability Assessment for Flow Imaging Microscopy Across Platforms. PubMed Central (PMC).
[4] United States Pharmacopeia (USP). General Chapter <1788> Methods for the Determination of Subvisible Particulate Matter, and <1788.3> Flow Imaging Method for the Determination of Subvisible Particulate Matter.
[5] Park, K. (2024/2025). PLGA-based long-acting injectable (LAI) formulations. Journal of Controlled Release / KP Publications.
[6] Khaled, et al. (2023). Synthesis of Gemcitabine-Loaded PLGA Microparticles with Green Solvents. ACS Omega, 8(35).
[7] 荆志宇, 李书, 霍珍妮, 等. 一种聚合物微球球内无菌的检测方法[P]. 中国专利: CN202410791571, 2024-09-06.
[8] Shibata, H., Harazono, A., Kiyoshi, M., et al. (2022). Quantitative Evaluation of Insoluble Particulate Matters in Therapeutic Protein Injections Using Light Obscuration and Flow Imaging Methods. Journal of Pharmaceutical Sciences, 111(3), 648-654.
